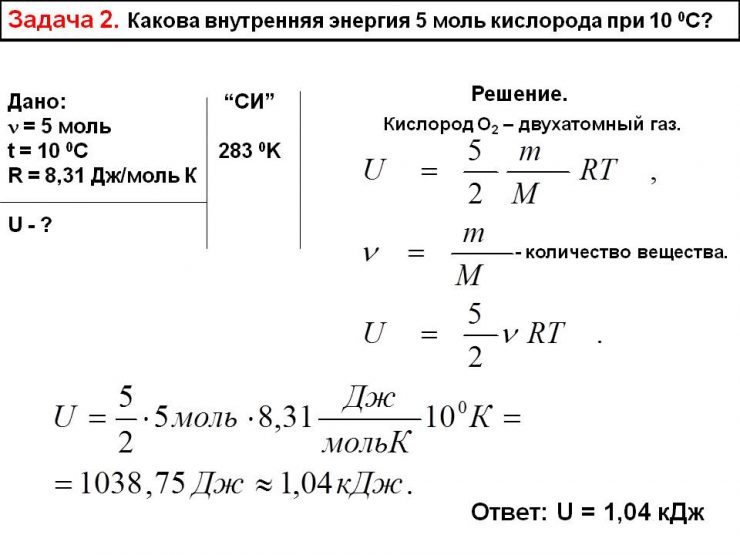
Содержание
- 1 Определите внутреннюю энергию 2 моль гелия при температуре 27 °С.
- 2 Какова температура одноатомного идеального газа, если известно, что внутренняя энергия
- 3 Задачи на внутреннюю энергию с решениями
- 4 1. На сколько изменилась внутренняя энергия одноатомного газа, количество вещества которого ν=10 моль, при его изобарном нагревании на ΔТ=100К? Какую работу совершил при этом газ и какое количество теплоты ему было сообщено? 2. В комнате объемом 200 м3 относительная влажность при 200С равна 70%. Определить массу водяных паров в воздухе комнаты. 3. 3. Углекислый газ массой 20г нагрет от температуры 290К до температуры 300К при постоянном давлении. Определите: 1) А(Дж)- работу, которую совершил газ при расширении; 2) ΔU(Дж)- изменение его внутренней энергии. ПОМОГИТЕ ПОЖАЛУЙСТА С ФИЗИКОЙ.
- 5 Внутренняя энергия 2 молей
- 6 Главная
- 7 Внутренняя энергия 2 молей
- 8 Внутренняя энергия 2 молей
- 9 СПАДИЛО.РУ
Определите внутреннюю энергию 2 моль гелия при температуре 27 °С.
Ваш ответ
Решение задачи:
Внутреннюю энергию одноатомного идеального газа (U) можно определить по формуле:
У частицы одноатомного газа имеется 3 степени свободы, поэтому в формуле фигурирует цифра 3. Также в этой формуле (R) – универсальная газовая постоянная, равная 8,31 Дж/(моль·К).
Выразим из формулы (1) искомую температуру газа (T):
Вопросы на тему «Внутренняя энергия тела»
Вопрос 1. Что такое внутренняя энергия?
Ответ. Для начала, внутренняя энергия чего? Бутылки с пивом, воздуха в шарике, тазика с водой? Все макроскопические тела обладают энергией, заключенной внутри них: атомы твердого тела колеблются в кристаллической решетке около положений равновесия, молекулы газа находятся в постоянном хаотическом движении и т.д.
Внутренняя энергия вещества – это энергия, которая складывается из кинетической энергии всех атомов и молекул, и потенциальной энергии их взаимодействия друг с другом.
Для идеального газа с числом степеней свободы i внутренняя энергия вычисляется по формуле:

Вопрос 2. От чего зависит внутренняя энергия идеального газа?
Ответ. Эта величина не зависит от объёма и определяется только температурой.
Вопрос 3. Как изменяется внутренняя энергия тела?
Ответ. Если тело совершает работу, его внутренняя энергия уменьшается. Например, газ передвигает поршень. Если же работа совершается над телом, то внутренняя энергия увеличивается.
Вопрос 4. Что такое функция состояния?
Ответ. Функция состояния – это один из параметров, которым можно описать термодинамическую систему. Функция состояния не зависит от того, как система пришла в то или иное состояние, а определяется несколькими переменными состояния.
Внутренняя энергия – это функция состояния термодинамической системы. В общем случае она зависит от температуры и объёма.
Вопрос 5. Можно ли изменить внутреннюю энергию тела, не совершая над ним работы?
Ответ. Да, еще один способ изменения внутренней энергии – теплопередача. В процессе теплопередачи внутренняя энергия тел изменяется.
Нужна помощь в решении задач по любой теме и других студенческих заданий? Профессиональный студенческий сервис поспособствует в выполнении работы вне зависимости от ее сложности.
Какова температура одноатомного идеального газа, если известно, что внутренняя энергия
Решение задач: внутренняя энергия
Прежде чем приступать к задачам на внутреннюю энергию тела, посмотрите общую памятку по решению физических задач. И пусть под рукой на всякий случай всегда будут основные физические формулы.
Задача №1. Изменение внутренней энергии
Условие
Воздушный шар объёмом 500 м3 наполнен гелием под давлением 105 Па. В результате нагрева температура газа в аэростате поднялась от 10 °С до 25 °С. Как увеличилась внутренняя энергия газа?
Решение
Для решения будем использовать формулу внутренней энергии идеального газа:

Массу гелия выразим из уравнения Клапейрона-Менделеева:

Тогда можно записать:

Ответ: 4 МДж.
Задача №2. Внутренняя энергия и работа
Условие
Азот массой 200 г расширяется изотермически при температуре 280 К, причем объём газа увеличивается в 2 раза. Найти:
- Изменение ∆U внутренней энергии газа.
- Совершенную при расширении газа работу А.
- Количество теплоты Q, полученное газом.
Решение
Так как процесс изотермический, то изменение внутренней энергии равно нулю, а работа равна количеству теплоты, полученному газом:

Ответ: 0; 11,6 кДж; 11,6 кДж.
Задача №3. Изменение внутренней энергии при изобарном и изохорном процессе
Условие
Кислород занимает объём V1= 3 л при давлении p1= 820 кПа. В результате изохорного нагревания и изобарного расширения газ переведён в состояние с объёмом V2= 4,5 л и давлением p2= 600 кПа. Найти количество теплоты, полученное газом; изменение внутренней энергии газа.
Решение
Теплота, подведенная к газу, идет на совершение работы и изменение внутренней энергии:

В изохорном и изобарном процессе соответственно:


Изменение внутренней энергии при изохорном процессе:

Изменение внутренней энергии при изобарном процессе:

Общее изменение внутренней энергии:

Ответ: 4,75 кДж.
Задача №4. Изменение внутренней энергии двухатомного газа
Условие
Кислород массой 2 кг занимает объём 6 м3 и находится под давлением 1 атм. Газ был нагрет сначала при постоянном давлении до объёма 13 м3, а затем при постоянном объёме – до давления 23 атм. Найти изменение внутренней энергии газа.
Решение
Изменение внутренней энергии находим по формуле:

Эту форму можно преобразовать, используя уравнение Клапейрона-Менделеева:

Ответ: 75,7 МДж.
Задача №5. Внутренняя энергия смеси газов
Условие
В закрытом сосуде находится масса m1 = 20 г азота и масса m2 = 32 г кислорода. Определить изменение ΔU внутренней энергии смеси газов при охлаждении ее на ΔТ = 28 К.
Решение
Определим количество молей азота и кислорода, а затем общее количество вещества в смеси соответственно:

Изменение внутренней энергии:

Знак «минус» означает, что внутренняя энергия уменьшается.
Ответ: -539 Дж.
решение вопроса
- Все категории
- экономические 42,694
- гуманитарные 33,415
- юридические 17,860
- школьный раздел 592,144
- разное 16,674
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Задачи на внутреннюю энергию с решениями

Доверь свою работу кандидату наук!
Решение задач – занятие, которое любит далеко не каждый. Здесь мы стараемся сделать так, чтобы оно занимало у вас поменьше времени без ущерба для качества самого решения. Тема этой статьи — задачи на внутреннюю энергию.
Подписывайтесь на наш телеграм и читайте полезные материалы для студентов каждый день!
Условие задачи:
Какова температура одноатомного идеального газа, если известно, что внутренняя энергия 2 моль составляет 54,2 кДж.
Задача №5.4.1 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Ответ: 1901,1 °C.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.

2. Термодинамической системе передано количество теплоты 200 Дж. Как изменилась внутренняя энергия системы, если при этом она совершила работу 400 Дж?

3. Стержень отбойного молотка приводится в движение сжатым воздухом. Масса воздуха в цилиндре за время хода поршня меняется от 0,1 до 0,5 г. Считая давление воздуха в цилиндре и температуру (27⁰C) постоянными, определите работу газа за один ход поршня. Молярная масса воздуха М = 0,029 кг/моль.

4. На одинаковые газовые горелки поставили два одинаковых плотно закупоренных сосуда вместимостью по 1 л. В одном сосуде находится вода, а в другом — воздух. Какой сосуд быстрее нагревается до 50 °С? Почему?

5. Предложен следующий проект вечного двигателя (рис. 13.12). Закрытый сосуд разделен на две половинки герметичной перегородкой, сквозь которую пропущены трубка и водяная турбина в кожухе с двумя отверстиями. Давление воздуха в нижней части больше, чем в верхней. Вода поднимается по трубке и наполняет открытую камеру. В нижней части очередная порция воды выливается из камеры турбины, подошедшей к отверстию кожуха. Почему данная машина не будет работать вечно?

6. Положительна или отрицательна работа газа в процессах 1—2, 2—3 и 3—1 на рисунке 10.5? Получает газ тепло или отдает в каждом из этих процессов?

7. Какое количество теплоты необходимо для изохорного нагревания гелия массой 4 кг на 100 К?

8. Вычислите увеличение внутренней энергии водорода массой 2 кг при изобарном его нагревании на 10 К. (Удельная теплоемкость водорода при постоянном давлении равна 14 кДж/(кг• К).)

9. В цилиндре компрессора сжимают идеальный одноатомный газ, количество вещества которого 4 моль. Определите, насколько поднялась температура газа за один ход поршня, если при этом была совершена работа 500 Дж. Процесс считайте адиабатным.

10. В калориметре находится вода массой 0,4 кг при температуре 10 °С. В воду положили лед массой 0,6 кг при температуре -40 ⁰С. Какая температура установится в калориметре, если его теплоемкость ничтожно мала?

11. Какой должна быть температура нагревателя, для того чтобы стало возможным достижение значения КПД тепловой машины 80%, если температура холодильника 27 °С?

12. В процессе работы тепловой машины за некоторое время рабочим телом было получено от нагревателя количество теплоты (Q1 = 1,5 •10 6 Дж, передано холодильнику Q2 = -1,2 • 10 6 Дж. Вычислите КПД машины и сравните его с максимально возможным КПД, если температуры нагревателя и холодильника соответственно равны 250 °С и 30 °С.
1. На сколько изменилась внутренняя энергия одноатомного газа, количество вещества которого ν=10 моль, при его изобарном нагревании на ΔТ=100К? Какую работу совершил при этом газ и какое количество теплоты ему было сообщено?
2. В комнате объемом 200 м3 относительная влажность при 200С равна 70%. Определить массу водяных паров в воздухе комнаты.
3. 3. Углекислый газ массой 20г нагрет от температуры 290К до температуры 300К при постоянном давлении. Определите: 1) А(Дж)- работу, которую совершил газ при расширении; 2) ΔU(Дж)- изменение его внутренней энергии.
ПОМОГИТЕ ПОЖАЛУЙСТА С ФИЗИКОЙ.
![]()
1.
Дано:
ν=10 моль
ΔΤ=100Κ
R=8,31 Дж/моль · К
_________________
ΔU-?
A-?
Q-?
Решение:
Q=ΔU+A — первое правило термодинамики.
1)
А=pΔV -работа.
рΔV=νRΔΤ
Отсюда:
А=νRΔΤ
А=10 · 8,31 · 100
А=8,31 · 10³ Дж
2)
ΔU=3/2 · ∨ · R · ΔT — изменение внутренней энергии
ΔU=3/2 · 10 · 8,31 · 100
ΔU=12,465 · 10³ Дж
Δ U≈1,2 · 10⁴ Дж
3)
Q=ΔU+А — количество теплоты
Q=1,2 · 10⁴ + 8,31 · 10³
Q=12 · 10³ + 8,31 · 10³
Q=20,31 · 10³ Дж
Q≈20 кДж
Ответ: А=8,31 · 10³ Дж
ΔU=1,2 · 10⁴ Дж
Q=20 кДж
2.
Дано:
V=200 м³
t=200°C
φ=70 %
________
m-?
Решение:
Массу определим, используя следующую формулу:
m=ρV (1)
Где m-масса водяных паров, ρ-плотность водяного пара, V-объем комнаты.
Плотность можно определить через относительную влажность воздуха φ:
φ=ρ/ρ₀ · 100 % ⇒ ρ=φρ₀/100 % (2)
Здесь ρ₀=17,3 г/м³ плотность насыщенного водяного пара при температуре 20°С.
Подставим формулу (2) в (1) и найдем массу:
m=φρ₀/100 % · V
m=70 · 17,3/100 · 200
m=2422 г
m≈2 кг
Ответ: m=2 кг
3.
Дано:
Процесс-изобарный
m=20 г=0,02 кг
Т₁=290 К
Т₂=300 К
R=8,31 Дж/моль · К
_____________________
А-?
ΔU-?
Решение:
При изобарном процессе при изобарном процессе газ совершает работу тепло поглощается. Первый закон термодинамики выглядит так:
Q=ΔU+A
Где A-работа газа.
Q=mc(t₂-t₁)
Здесь с=920 Дж/кг · °С -удельная теплоемкость углекислого газа при постоянном давлении.
Температура равна:
t=T-273
t₁=T₁-273=290-273=17°С
t₂=T₂-273=300-273=27°С
Теперь найдем количество теплоты:
Q=0,02 · 920 · (27-17)
Q=184 Дж
Теперь найдем ΔU по формуле:
ΔU=3/2 · ∨ · R · ΔT
Где ν=m/M
Здесь М-молярная масса углекислого газа, находится по формуле:
M=Mr · 10⁻³
Mr(CO₂)=12+16 · 2=44
M=44 · 10⁻³ кг/моль
Итак:
ν=0,02/44 · 10⁻³
ν≈4,5
Теперь найдем ΔU:
ΔU=3/2 · 4,5 · 8,31 · (30-290)
ΔU≈561 Дж
Теперь, зная количество теплоты и изменение внутренней энергии найдем работу газа:
Q=ΔU+A
A=Q-ΔU
A=184-561
A=-377 Дж
Внутренняя энергия 2 молей


4. Необходимо расплавить лёд массой 0,2 кг, имеющий температуру 0 о С. Выполнима ли эта задача, если потребляемая мощность нагревательного элемента – 400 Вт, тепловые потери составляют 30%, а время работы нагревателя не должно превышать 5 минут?
Образец возможного решения
4*. Теплоизолированный горизонтальный сосуд разделён пористой перегородкой на две равные части. В начальный момент в левой части сосуда находится ν = 2 моль гелия, а в правой – такое же количество моль аргона. Атомы гелия могут проникать через перегородку, а для атомов аргона перегородка непроницаема. Температура гелия равна температуре аргона: Т = 300 К. Определите отношение внутренних энергий газов по разные стороны перегородки после установления термодинамического равновесия.
Образец возможного решения
4**. Теплоизолированный цилиндр разделён подвижным теплопроводным поршнем на две части. В одной части цилиндра находится гелий, а в другой – аргон. В начальный момент температура гелия равна 300 К, а аргона – 900 К; объёмы, занимаемые газами, одинаковы, а поршень находится в равновесии. Поршень медленно перемещается без трения. Теплоёмкость поршня и цилиндра пренебрежимо мала. Чему равно отношение внутренней энергии гелия после установления теплового равновесия к его энергии в начальный момент?
Образец возможного решения

6. В горизонтальном цилиндрическом сосуде, закрытом поршнем, находится одноатомный идеальный газ. Первоначальное давление газа p1 = 4•10 5 Па. Расстояние от дна сосуда до поршня равно L. Площадь поперечного сечения поршня S = 25 см 2 . В результате медленного нагревания газ получил количество теплоты Q = 1,65 кДж, а поршень сдвинулся на расстояние x = 10 см. При движении поршня на него со стороны стенок сосуда действует сила трения величиной Fтр = 3•10 3 Н. Найдите L. Считать, что сосуд находится в вакууме.
Образец возможного решения

8. 10 моль одноатомного идеального газа сначала охладили, уменьшив давление в 3 раза, а затем нагрели до первоначальной температуры 300 К (см. рисунок). Какое количество теплоты получил газ на участке 2 — 3?
Образец возможного решения

9. 10 моль идеального одноатомного газа охладили, уменьшив давление в 3 раза. Затем газ нагрели до первоначальной температуры 300 К (см. рисунок). Какое количество теплоты сообщено газу на участке 2 — 3?
Образец возможного решения

10. 1 моль идеального одноатомного газа сначала охладили, а затем нагрели до первоначальной температуры 300 К, увеличив объем газа в 3 раза (см. рисунок). Какое количество теплоты отдал газ на участке 1 — 2?
Образец возможного решения

10*. Над одноатомным идеальным газом проводится циклический процесс, показанный на рисунке. На участке 1–2 газ совершает работу А12 = 1000 Дж. На адиабате 3–1 внешние силы сжимают газ, совершая работу |A31| = 370 Дж. Количество вещества газа в ходе процесса не меняется. Найдите количество теплоты |Qхол|, отданное газом за цикл холодильнику.
Образец возможного решения
Главная
От создателя:
Очень часто мне приходилось проводить бесследно потеряные часы за поисками книг и научных работ всвязи с необходимостью написания рефератов, дипломных, диссертаций. Я искал книги в библиотеках и в интернете. Во время этих поисков, я понял насколько трудно в наше время найти нормальные источники информации, на которые можно было бы опереться в ходе написания научных работ. Проблема заключается в том, что в библиотеке усложнена система поиска — приходится механически перебирать очень много книг, а в интернете слишком много рекламы и когда натыкаешься на долгожданную нужную книгу, тебе её тут же предлагают купить! Но разве нужна Вам эта книга из 400 или более страниц, если нужно-то из неё всего одна глава или вообще обзац текста — для того, чтобы понять смысл, мнение того или иного автора относительно той или иной проблемы, и сослаться на его работу. Без злого умысла плагиата или воровства интеллектуального имущества. Наоборот, для освещения работы автора, использования по назначению его не напрасных трудов. Разве знания не должны быть более доступны для более прогрессивного развития общества?
Именно поэтому и был создан этот проект — чтобы помочь тем, кто нуждается в помощи, подобно тому, как я нуждался в ней. Здесь выложены книги в черновом текстовом варианте, чтобы, используя поиск, вы могли найти нужную информацию и сослаться на определённую книгу определённого автора. Теперь не придётся покупать книги, не зная, пригодятся они Вам или нет.
Следует отметить, что страницы на сайте могут не совпадать со страницами книги, так как книги на сайте искусственно поделены на примерно равные части для удобства поиска, чтения и меньшей загрузки браузера. Также не стоит браниться относительно ошибок в тексте или неверным отображением формул (разделы химии, математики, физики и др..). Напомню, что текст выложен для того, чтобы Вы могли найти и скачать нужную Вам книгу. Если же Вы желаете исправить данное упущение, то ваша помощь проекту приветствуется — Ваши старания не оставят равнодушными очень многих людей.
Также есть возможность скачать книги в электронном варианте для более подробного изучения.
На данный момент на сайте доступны работы следующих авторов:
Внутренняя энергия 2 молей
Какую работу совершил идеалный одноатомный газ и как при этом изменилась его внутренняя энергия при изобарном нагревании 2 молей газа на 50К? Какое кол-во теплоты получил газ в процессе теплообмена?
Согласно первому закону термодинамики при изобарном процессе теплота расходуется на изменение внутренней энергии и работу газа Q=∆U+A.
Работа газа в изобарном процессе равна: А =P∆V= νR∆T = 2*8.31*50 = 831Дж
Изменение внутренней энергии для идеального одноатомного газа
∆U= 3/2*νR∆T=3/2 * 2*8.31*50 =1246.5 Дж
Q=1246.5 + 831 =2077.5 Дж
Ответ 831Дж ; 1246.5 Дж ; 2077.5 Дж
Внутренняя энергия 2 молей
Тема 2. Молекулярная физика и термодинамика.
Молекулярная физика
Основные понятия
Количество вещества измеряется в молях (n).
n — число молей
1 моль равен количеству вещества системы, содержащей столько же частиц, сколько атомов содержится в 0,012 кг углерода  . Число молекул в одном моле вещества численно равно постоянной Авогадро NA.
. Число молекул в одном моле вещества численно равно постоянной Авогадро NA.

Идеальный газ. Основное уравнение молекулярно-кинетической теории.
Основным уравнением молекулярно-кинетической теории газа является уравнение:
Уравнение Клапейрона-Менделеева, изопроцессы.
Состояние идеального газа характеризуют давлением р, объемом V, температурой Т.
[p]=Паскаль (Па), [V]=м3, [T]=Кельвин (К).
Уравнение состояния идеального газа:
1. Если m=const, T=const – изотермический процесс.
Уравнение процесса: 

2. Если m=const, V=const – изохорический процесс.
Уравнение процесса:  .
.

3. Если m=const, p=const – изобарический процесс.
Уравнение процесса: 

4. Адиабатический процесс – процесс, протекающий без теплообмена с окружающей средой. Это очень быстрый процесс расширения или сжатия газа.
Насыщенный пар, влажность.
Абсолютная влажность – давление р водяного пара, содержащегося в воздухе при данной температуре.
Относительная влажность – отношение давления р водяного пара, содержащегося в воздухе при данной температуре, к давлению ро насыщенного водяного пара при той же температуре:

Термодинамика
Термодинамика изучает наиболее общие закономерности превращения энергии, но не рассматривает молекулярного строения вещества.
Всякая физическая система, состоящая из огромного числа частиц – атомов, молекул, ионов и электронов, которые совершают беспорядочное тепловое движение и при взаимодействии между собой обмениваются энергией, называется термодинамической системой. Такими системами являются газы, жидкости и твердые тела.
Внутренняя энергия.
Термодинамическая система обладает внутренней энергией U. При переходе термодинамической системы из одного состояния в другое происходит изменение ее внутренней энергии.
Изменение внутренней энергии идеального газа равно изменению кинетической энергии теплового движения его частиц.
Изменение внутренней энергии DU при переходе системы из одного состояния в другое не зависит от процесса, по которому совершался переход.
Для одноатомного газа:
Работа в термодинамике.
Первый закон термодинамики.
Закон сохранения энергии в термодинамике называют: первый закон термодинамики.
Первый закон термодинамики:


КПД тепловой машины.
Тепловой машиной называется периодически действующий двигатель, совершающий работу за счет получаемого извне количества теплоты. Тепловая машина должна состоять из трех частей: 1) рабочего тела – газа (или пара), при расширении которого совершается работа; 2) нагревателя – тела, у которого за счет теплообмена рабочее тело получает количество теплоты Q1; 3) холодильника (окружающей среды), отбирающего у газа количество теплоты Q2.
Нагреватель периодически повышает температуру газа до Т1, а холодильник понижает до Т2.
Отношение полезной работы А, выполненной машиной, к количеству теплоты, полученной от нагревателя, называется коэффициентом полезного действия машины h:



ТЕСТОВЫЕ ЗАДАНИЯ
- Какое число молекул содержит 1 моль кислорода?
- Получите из уравнения Менделеева-Клапейрона уравнение изобарического процесса.
- По графикам изопроцессов в координатных осях V-T постройте графики тех же процессов в координатных осях p-V.

- Определите температуру в состоянии В, если в состоянии А Т=200 К.

- Два сосуда объемами V1 и V2 заполнены идеальным газом при давлении р1 и р2. Какое установится давление в сосудах, если их соединить между собой? Температура не изменяется.
- Докажите, что удельная теплоемкость газа при постоянном давлении больше, чем при постоянном объеме.
- Идеальному газа передается количество теплоты таким образом, что в любой момент времени переданное количество теплоты Q равно работе А, совершенной газом. Какой процесс осуществлен?
- Идеальный газ переходит из состояния М в состояние N тремя различными способами, представленными на диаграмме p-V. В каком случае работе будет минимальной?

- Идеальному газу передано количество теплоты 5 Дж и внешние силы совершили над ним работу 8 Дж. Как изменится внутренняя энергия газа?
- Каково максимально возможное КПД тепловой машины, использующей нагреватель с температурой 427о С и холодильник с температурой 27о С.
Ответы и решения
- Моль любого вещества содержит одинаковое число молекул, равное числу Авогадро:

СПАДИЛО.РУ
Термодинамика
В задании №9 ЕГЭ по физике необходимо продемонстрировать знания в области такого раздела физики, как термодинамика. Работа идеального газа, КПД тепловых машин, циклы — вот, что ждет нас в девятом задании.
Теория к заданию № 9 ЕГЭ по физике
Работа идеального газа
Пусть газ находится в сосуде, в котором есть поршень. Работа равна произведению силы на перемещение: A=F(h1 – h2).
Сила давления на стенки сосуда и поршень равна произведению давления газа p на площадь поверхности S. Тогда работа газа равна
Следовательно, газ выполняет работу, если изменяется его объём.
При постоянном давлении работа –это произведение давления и разности объёмов.

Молекулы газа обладают кинетической энергией и при сильном сжатии газа ведут себя как упругие тела. Это означает, что они обладают ещё и потенциальной энергией. Кинетическая и потенциальная энергия молекул, из которых состоит газ, в сумме составляют внутреннюю энергию газа U.
Внутренняя энергия газа может быть рассчитана по формуле:

где ν – кол-во вещество, измеряемое в молях; R – универсальная газовая постоянная (R=8,31 Дж/(моль·К)); T – температура газа.
Если изменять одновременно температуру Т и давление р с объёмом V, разобраться в закономерностях изменения состояния газа тяжело.
Газовые процессы
- Изобарный процесс происходит при постоянном давлении, т.е. p = const. При нем теплота Q затрачивается на увеличение объёма газа и повышение температуры.
- Изохорный процесс происходит при поддержании постоянного объема, т.е. при V = const. Работа в данном случае не выполняется, а теплота, получаемая газом, затрачивается на изменение внутренней энергии.
- Изотермический проходит при постоянной температуре (T=const). В этом случае теплота идёт на изменение объёма, то есть на выполнение работы. При изотермическом процессе Q = А.
Графики газовых процессов изображены на рисунках ниже. 
Количество теплоты, которое необходимо затратить при нагревании тела массой т, на Δt градусов, определяется формулой Q=cmΔt. Здесь с – удельная теплоемкость материала, из которого изготовлено тело.
КПД тепловой машины

Здесь Q1 – количество теплоты, полученное от нагревателя, Q2 – количество теплоты,которое отдано холодильнику, A- полезная работа.
Разбор типовых заданий №9 ЕГЭ по физике
Демонстрационный вариант 2018
На ТV-диаграмме показан процесс изменения состояния идеального одноатомного газа. Газ получил количество теплоты, равное 50 кДж. Какую работу совершил газ в этом процессе, если его масса не меняется?

Алгоритм решения:
- Анализируем условие задачи. Записываем уравнение 1-го закона термодинамики.
- Записываем формулу для расчета внутр.энергии. Находим ее значение.
- Определяем работу,
Решение:
1. По условию задачи газ получил 50 кДж теплоты. После этого газ выполнил работу.По 1-му закону термодинамики Q=A+∆U (1)
2. ∆U можно найти из уравнения: ∆ = 3/2 ∆ , поскольку на графике представлена зависимость объема от температуры. Видно, что процесс, изображенный на рисунке, является изотермическим, т.е. Т1=Т2. А это в свою очередь означает, что ∆Т=Т2–Т1=0 и, следовательно, ∆U=0.
3. Получаем из (1): A=Q=50 кДж
Первый вариант задания (Демидова, №1)
На рТ-диаграмме показан процесс изменения состояния 4 моль идеального газа. Внутренняя энергия газа увеличилась на 40 кДж. Какую работу совершил газ в этом процессе?

Алгоритм решения:
- Анализируем задание и график, на котором изображен газовый процесс.
- Устанавливаем вид процесса.
- Определяем работу, которая выполняется в данном случае.
- Записываем ответ.
Решение:
1. Из рисунка видно, что давление прямо пропорционально зависит от температуры, т.е. p=αT, Здесь α – некоторый коэффициент. Согласно уравнению Менделеева – Клапейрона имеем:
 Отсюда
Отсюда 
2. Значит, процесс изохорный. При нем объем не меняется.
3. Работа газа всегда связана расширением или сжатием газа, чего в данном случае не происходит. Значит, работа при этом не производится. Она равна 0.
Второй вариант задания (Демидова, №8)
Кусок алюминия массой 5 кг нагрели от 20 °С до 100 °С. Какое количество теплоты было затрачено на его нагрев?
Алгоритм решения:
- Записываем формулу для определения количества теплоты.
- Вычисляем количество теплоты, подставив приведенные в условии значения величин.
- Записываем ответ.
Решение:
1. Количество теплоты Q, которое затрачивается на нагревание куска определяется по формуле: Q=cmΔt.
2. Масса тела по условию равна т=5 кг, теплоемкость алюминия равна с = 900 Дж/(кг· 0 С), а разность температур Δt = 100 0 -20 0 = 80 0 .
Имеем: Q= 900∙5∙80= 360000Дж =360 кДж.
Третий вариант задания (Демидова, №28)
Тепловая машина с КПД 40 % совершает за цикл полезную работу 60 Дж. Какое количество теплоты машина получает за цикл от нагревателя?
Алгоритм решения:
- Записываем формулу КПД для тепловой машины.
- Подставляем числовые значения и вычисляем требуемое количество теплоты.
- Записываем ответ.
Решение:
1. КПД тепловой машины вычисляется по формуле: 
где Q1 – количество теплоты, которое получает тепловая машина от нагревателя; А – полезная работа. По условию A = 60 Дж. А коэффициент полезного действия равен 40%= 0,4. Из формулы получаем:
 Ответ: 150
Ответ: 150
Источники
- http://zaochnik.ru/blog/zadachi-na-vnutrennjuju-energiju-s-reshenijami/
- http://www.soloby.ru/884418/%D0%BE%D0%BF%D1%80%D0%B5%D0%B4%D0%B5%D0%BB%D0%B8%D1%82%D0%B5-%D0%B2%D0%BD%D1%83%D1%82%D1%80%D0%B5%D0%BD%D0%BD%D1%8E%D1%8E-%D1%8D%D0%BD%D0%B5%D1%80%D0%B3%D0%B8%D1%8E-%D0%BC%D0%BE%D0%BB%D1%8C-%D0%B3%D0%B5%D0%BB%D0%B8%D1%8F-%D0%BF%D1%80%D0%B8-%D1%82%D0%B5%D0%BC%D0%BF%D0%B5%D1%80%D0%B0%D1%82%D1%83%D1%80%D0%B5
- http://easyfizika.ru/zadachi/termodinamika/kakova-temperatura-odnoatomnogo-idealnogo-gaza-esli-izvestno-chto-vnutrennyaya-energiya/
- http://gdz-fizika.ru/5/97-uprazhnenie-15.html
- http://dvoechka.com/fizika/dv160143.html
- http://xn--80aaehfbdnibse7ai3audo8byp.xn--p1ai/ege/uroven_C/termodinamika_C/termodinamika_C.html
- http://www.booksshare.net/index.php?author=turchina-nv&book=2008&category=physics&id1=4&page=72
- http://fizikahelp.ru/91/916/5343.html
- http://www.sites.google.com/a/ssga.ru/ssga4school/fizika/tema-2
- http://spadilo.ru/zadanie-9-ege-po-fizike/